Comunicato stampa n. 686 – L’Agenzia Italiana del Farmaco ha pubblicato il Rapporto annuale sulla sicurezza dei vaccini anti-COVID-19. I dati raccolti e analizzati riguardano le segnalazioni di sospetta reazione avversa 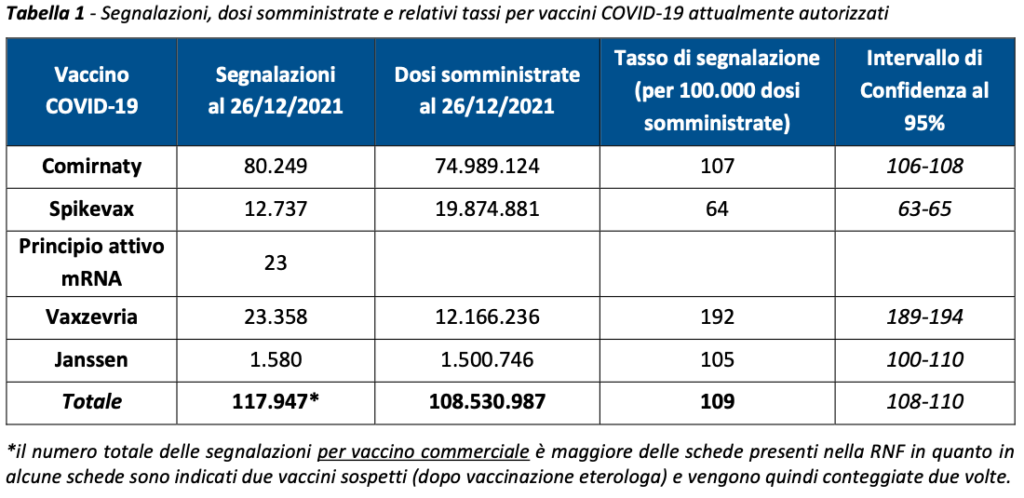
They were received during the period in question 117.920 segnalazioni out of a total of 108.530.987 di dosi administered (reporting rate of 109 ogni 100.000 dosi), of which the83,7% (n. 98.717) riferite a eventi non gravi, come dolore in sede di iniezione, febbre, astenia/stanchezza, dolori muscolari, con un tasso di 17,6 eventi gravi ogni 100.000 dosi somministrate. Come riportato nei precedenti Rapporti, indipendentemente dal vaccino, dalla dose e dalla tipologia di evento, la reazione si è verificata nella maggior parte dei casi (73% circa) nella stessa giornata della vaccinazione o il giorno successivo e solo più raramente oltre le 48 ore.
Nell’anno di campagna vaccinale Comirnaty [Pfizer/BioNTech) è stato il vaccino più utilizzato in Italia (69,1%), seguito da Spikevax [Moderna] (18,3%), Vaxzevria [AstraZeneca] (11,2%), e Vaccino COVID-19 Janssen (1,4%). Le segnalazioni per tipologia di vaccino sono invece così distribuite: Comirnaty 68%, Vaxzevria 19,8%, Spikevax 10,8%, Vaccino COVID-19 Janssen 1,4%.
Per tutti i vaccini gli eventi avversi più segnalati, perlopiù non gravi e già risolti al momento della segnalazione, sono febbre, stanchezza, cefalea, dolori muscolari/articolari, dolore in sede di iniezione, brividi e nausea. Si segnala che nell’ambito degli studi registrativi fino a un 64% di effetti indesiderati è stato rilevato nel gruppo placebo ed è riferibile al cosiddetto effetto nocebo.
Per quanto riguarda la somministrazione della third dose, iniziata nel mese di settembre, al 26 dicembre 2021 sono state inserite nella RNF 3.510 segnalazioni, a fronte di 16.198.231 di terze dosi administered, with a reporting rate of 21,7 segnalazioni ogni 100.000 terze dosi, inferiore a quanto osservato per le dosi del ciclo primario. L’84,1% (n. 2.951) delle segnalazioni è riferita a eventi non gravi, con un tasso di segnalazione pari a 18,2 ogni 100.000 dosi somministrate, e il 15,9% (558) a eventi avversi gravi, con un tasso di 3,4 segnalazioni di eventi gravi ogni 100.000 dosi somministrate.
In merito alle vaccinazioni in età pediatrica (5-16 anni), al 26/12/2021 risultano somministrate 4.178.361 di dosi di vaccino, il 96% delle quali nella fascia di età 12-16 anni (4.005.471 dosi) e il 4% nella fascia 5-11 anni (172.890 dosi). Tra i due vaccini autorizzati per questa popolazione, Comirnaty è stato il più utilizzato (87,5%) (Spikevax 12,5%). Al 26 dicembre 2021 nella RNF sono state registrate complessivamente 1.170 segnalazioni di sospette reazioni avverse manifestatesi nella popolazione pediatrica, che rappresentano l’1% di tutte le segnalazioni, con un tasso di segnalazione pari a 28 eventi ogni 100.000 dosi somministrate nella fascia pediatrica, indipendentemente dalla tipologia di vaccino e dalla valutazione del nesso di causalità, inferiore dunque rispetto a quello riscontrato nella popolazione generale (109 eventi ogni 100.000 dosi somministrate). Nella popolazione pediatrica gli eventi avversi più frequentemente segnalati sono febbre, cefalea, stanchezza e vomito. Il 69% delle reazioni si sono risolte completamente o erano in miglioramento al momento della segnalazione. I tassi di segnalazione nella fascia d’età 5-11 sono preliminari e al momento non emergono particolari problemi di sicurezza.
There vaccinazione per COVID-19 è indicata sia in gravidanza sia in allattamento e non emergono particolari problemi di sicurezza dai dati di farmacovigilanza e di studi ad hoc in questa popolazione. Non vi sono inoltre evidenze che suggeriscano che i vaccini anti-COVID-19 possano influenzare negativamente la fertilità in entrambi i sessi.
Gli altri approfondimenti presenti nel Rapporto, su eventi di particolare interesse come anafilassi, sindrome di Guillain-Barré, miocarditi/pericarditi, paralisi di Bell e trombosi trombocitopenica confermano i dati di sicurezza valutati a livello europeo.
AIFA – Pubblicato il: 09 febbraio 2022
