
È stato presentato alla Conferenza Stato Regioni e Province Autonome il Piano di attività per l’anno 2022 che  espone le linee di indirizzo relative all’attività dell’AIFA: tali linee d’indirizzo sono state individuate dalla Direzione Generale dell’Agenzia (“DG”), nel contesto della più e ampia programmazione operativa e organizzativa relativa al periodo 2022-2024.
espone le linee di indirizzo relative all’attività dell’AIFA: tali linee d’indirizzo sono state individuate dalla Direzione Generale dell’Agenzia (“DG”), nel contesto della più e ampia programmazione operativa e organizzativa relativa al periodo 2022-2024.
AIFA precisa che la definizione del Piano è avvenuta, in primo luogo, sulla base di un proficuo e continuo confronto con il MinSal e la Conferenza Stato-Regioni (“Conferenza”), tenuto conto degli obiettivi istituzionali assegnati all’Agenzia mediante la Direttiva generale del Ministro all’AIFA pervenuta i 22 settembre 2021 e alla luce dei più recenti atti di indirizzo in materia di governance farmaceutica adottati a livello nazionale e dell’Unione Europea (“UE”).
Con specifico riferimento all’ambito UE, va rilevato come a seguito della Pharmaceutical Strategy for Europe lanciata nel novembre 2020 dalla Commissione sia stato avviato un ampio processo di revisione del diritto farmaceutico dell’Unione, comprensivo di un confronto con principali portatori d’interessi
Missione fondamentale dell’AIFA è, dunque, garantire l’accesso universale a farmaci sicuri ed efficaci nel SSN in modo equo e sostenibile: l’Agenzia contribuisce alla tutela del diritto alla salute garantito dall’articolo 32 della Costituzione attraverso l’unitarietà delle attività in materia di farmaceutica, il monitoraggio del consumo e della spesa farmaceutica e la promozione in Italia dell’informazione indipendente e degli investimenti in ricerca e sviluppo.
L’Agenzia persegue il proprio mandato istituzionale mediante l’attuazione delle direttrici strategiche, che vengono declinate sotto forma di obiettivi generali triennali (obiettivi strategici) ed obiettivi specifici annuali (obiettivi operativi), i cui contenuti coincidono con quanto presentato nel “Piano di attività annuale per l’anno 2022” dell’AIFA.
Sono stati coinvolti, contribuendo alla stesura del documento, tutti i dirigenti responsabili delle Strutture dell’Agenzia con il coordinamento dell’Ufficio Controllo di Gestione.
L’AIFA ha strutturato il Piano della Performance 2022-2024, in coerenza con i vincoli di bilancio, per la programmazione economico-finanziaria del triennio 2022-2024 si rinvia al paragrafo “Budget”.
Nel Piano troviamo: Rinegoziazioni e contratti, appropriatezza prescrittiva, potenziamento delle liste dl trasparenza, maggiore uso dei biosimilari, semplificazione importazioni parallele, più velocità nell’approvazione dei farmaci, equivalenza terapeutica, riduzione prezzi convenzionata, revisione prontuario, regole omogenee per la distribuzione diretta e per conto e maggiore dialogo con le Regioni.
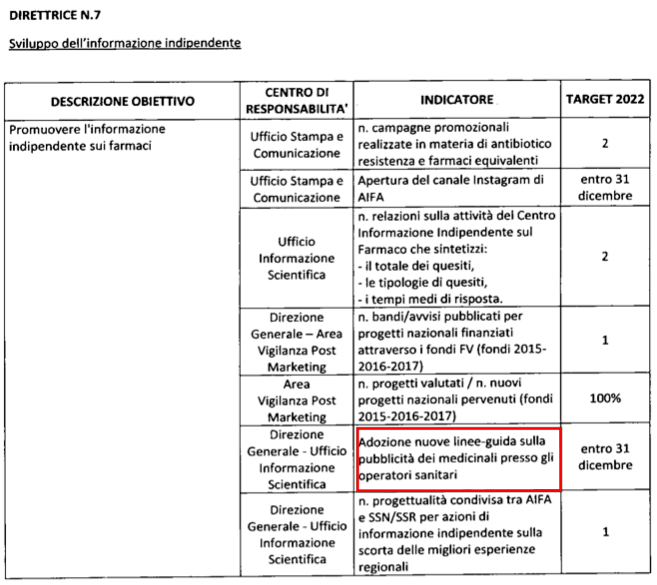 Nella Direttrice 7 del Piano per il 2022 troviamo a pagina 22 “Sviluppo dell’Informazione indipendente” nell’ambito del quale, a cura della Direzione Generale (Ufficio Informazione Scientifica) c’è “Adozione nuove linee-guida sulla pubblicità dei medicinali presso gli operatori sanitari” da attuarsi entro il 31 dicembre. Ovviamente le nuove linee guida AIFA sull’informazione scientifica (con 16 anni di ritardo da quanto stabilito dal D.Lgs. 219/06) vengono fatte senza consultare i diretti interessati, quelli che in pratica e concretamente svolgono quel tipo di attività, cioè gli informatori scientifici del farmaco. È fatta da persone dotate certamente di buona volontà che sicuramente conoscono leggi e direttive europee, dopo aver consultato le industrie farmaceutiche (la cui visione è prevalentemente commerciale), ma altrettanto sicuramente non hanno mai visto un informatore scientifico e quindi senza poter cogliere le varie sfaccettature con cui si svolge quotidianamente questo tipo di attività. Senza queste conoscenze le “nuove linee guida” rischiano di essere l’ennesimo documento destinato all’irrilevanza. Diceva l’ormai purtroppo dimenticato Einaudi: “Giova deliberare senza conoscere?“
Nella Direttrice 7 del Piano per il 2022 troviamo a pagina 22 “Sviluppo dell’Informazione indipendente” nell’ambito del quale, a cura della Direzione Generale (Ufficio Informazione Scientifica) c’è “Adozione nuove linee-guida sulla pubblicità dei medicinali presso gli operatori sanitari” da attuarsi entro il 31 dicembre. Ovviamente le nuove linee guida AIFA sull’informazione scientifica (con 16 anni di ritardo da quanto stabilito dal D.Lgs. 219/06) vengono fatte senza consultare i diretti interessati, quelli che in pratica e concretamente svolgono quel tipo di attività, cioè gli informatori scientifici del farmaco. È fatta da persone dotate certamente di buona volontà che sicuramente conoscono leggi e direttive europee, dopo aver consultato le industrie farmaceutiche (la cui visione è prevalentemente commerciale), ma altrettanto sicuramente non hanno mai visto un informatore scientifico e quindi senza poter cogliere le varie sfaccettature con cui si svolge quotidianamente questo tipo di attività. Senza queste conoscenze le “nuove linee guida” rischiano di essere l’ennesimo documento destinato all’irrilevanza. Diceva l’ormai purtroppo dimenticato Einaudi: “Giova deliberare senza conoscere?“
Il Piano, dice l’Agenzia, è comunque uno strumento fondamentale per gestire la spesa farmaceutica è la rinegoziazione dei prezzi al momento della scadenza di ogni accordo negoziale. L’AIFA ha attivato un monitoraggio sistematico dei contratti in scadenza evitando (come spesso accadeva) il tacito rinnovo post scadenza.
Le note sono uno strumento per regolamentare l’utilizzo dei farmaci, promuovere l’appropriatezza
prescrittiva tenendo conto delle nuove evidenze scientifiche/nuove pratiche cliniche che via via si
presentano. La gestione attraverso le note di appropriatezza, infatti, permette ad AIFA di controllare
l’impatto economico rinegoziando i prezzi. Tra le Nota AIFA di maggior successo in termini di
recupero di appropriatezza prescrittiva si segnala la Nota 96 sulla Vitamina D che ha anche prodotto
una riduzione di spesa di circa 50 milioni di euro anno.
L’introduzione della procedura semplificata sia per farmaci equivalenti/biosimilari (generici)” sia
per le importazioni parallele ha determinato una riduzione delle tempistiche di valutazione pari al
15%. A questo dato si associa una risposta positiva delle aziende farmaceutiche che hanno preferito
tale procedura rispetto alla negoziazione ordinaria disciplinata. Infatti, nel 2021 l’89% delle
procedure aventi ad oggetto farmaci generici si è svolta secondo le modalità di negoziazione
semplificata.
Inoltre, la procedura semplificata di negoziazione del prezzo e di rimborso dei farmaci di
importazione parallela, che ha riaperto al mercato tali medicinali facendo registrare, nel 2021, 111
procedure semplificate valutate in un tempo medio pari a 47 giorni.
Nella revisione del prontuario rientrano non solo le azioni precedentemente illustrate (si vedano i
precedenti paragrafi relativi a: RINEGOZIAZIONI e CONTRATTI; NOTE AIFA; LISTE DI TRASPARENZA;
EQUIVALENZA TERAPEUTICA/SOVRAPPONIBILITA’ e RIALLINEAMENTO DEI PREZZI NELLA
CONVENZIONATA), alcune delle quali già poste in essere o programmate, ma anche l’ammissione
alla rimborsabilità di categorie attualmente in fascia C (in primis i COC, Contraccettivi ormonali combinati) o anche l’esclusione dalla rimborsabilità di categorie di farmaci con un uso cresciuto o fuori controllo. Tutto ciò rappresenta un valido strumento di governo della spesa, soprattutto considerando la possibilità di escludere
dalla rimborsabilità quei farmaci i quali, a seguito di specifica istruttoria e valutazione, hanno mostrato nel tempo un profilo beneficio/rischio modesto o limitato.
Il Piano ha come obiettivo la riduzione del 10% dello sfondamento, con il contemporaneo contenimento entro il 5% dell’incremento della spesa complessiva.
In assoluto, osserva AIFA, dal 2013 al 2024, per la spesa farmaceutica si sono allocate risorse. economiche aggiuntive pari a circa 3,7 miliardi di euro ed è stata allocata una maggiore quota di finanziamento sugli acquisti diretti.
Con queste manovre (aumento delle risorse e rimodulazione tetto acquisti diretti) di fatto si potrà tendere a far 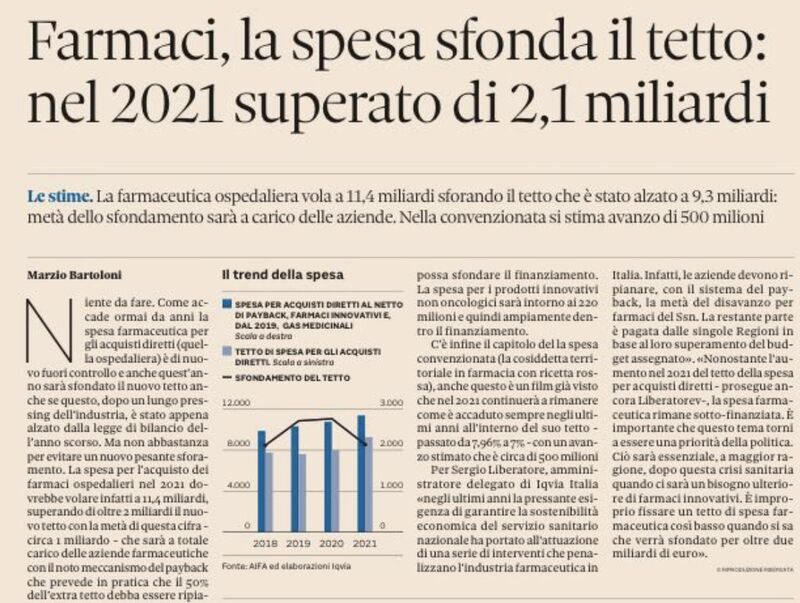 coincidere la spesa farmaceutica con le risorse assegnate (come quota parte del FSN), con possibile progressiva riduzione dello sfondamento anche grazie ad una serie di azioni virtuose elencate nel Piano.
coincidere la spesa farmaceutica con le risorse assegnate (come quota parte del FSN), con possibile progressiva riduzione dello sfondamento anche grazie ad una serie di azioni virtuose elencate nel Piano.
L’effetto osservato è quello di un progressivo riequilibrio tra risorse non spese nella convenzionata ed eccesso di spesa nel canale degli acquisti diretti; ciò si traduce quindi in una riduzione dello sfondamento del tetto degli acquisiti diretti il cui ripiano è coperto al 50% da aziende farmaceutiche e regioni. Infatti, dal 2019 in cui si è assistito ad uno sfondamento degli acquisti diretti di oltre 2,7 miliardi si è arrivati ad uno sfondamento nel 2021 che verosimilmente è di circa 2 miliardi e si può prevedere nel 2023, a normativa vigente, una riduzione dello sfondamento riportandolo a circa miliardo.
Conclusioni del documento
- la spesa farmaceutica è stabile nell’ultimo triennio 2019-2021 e costantemente monitorata;
- le manovre attuate progressivamente portano, nel prossimo triennio 2022-2024, ad un riequilibrio della spesa con le risorse programmate per i due canali di erogazione;
- le leve più importanti già attuate per garantire la sostenibilità del SSN/SSR sono: rinegoziazioni; note AIFA di appropriatezza; potenziamento lista di trasparenza; lista legge 648 e semplificazione e importazioni parallele;
- Altre leve disponibili saranno attuate con applicazione della Legge di Bilancio 2022: riallineamento prezzi, revisione Prontuario ed equivalenza/sovrapponibilità terapeutica. Tali azioni aggiuntive dovranno essere oggetto di programmazione congiunta Stato/Regioni.
- Utile richiamare come leve importanti per la sostenibilità della spesa SSN/SSR, che non sono sotto il diretto controllo di AIFA, sono associate, in particolare, alle forti differenze legate alla variabilità regionale
- Su alcuni ambiti strategici occorre sviluppare strategie di migliore implementazione a livello regionale/locale per colmare possibili gap esistenti di appropriatezza di variabilità: implementazione/ottimizzazione procedure di acquisto; obiettivi condivisi con DG asl/ospedali; audit da parte di commissioni di appropriatezza.
- Il problema del prezzo troppo elevato di alcuni farmaci va visto e affrontato in un’ottica internazionale in quanto il farmaco e il mercato farmaceutico sono beni globali regolati : più livelli: globale, continentale (EU) e locale (nazionale e regionale). Recenti iniziative governative come la Oslo Medicines Inititative (OMI) mirano a coordinare azioni globali per una maggiore accessibilità ai farmaci innovativi e l’Italia ne parte attiva.
- Un maggiore dialogo con le regioni (non solo quelle in piano di rientro) può consentire importanti margini di ulteriore efficientamento del sistema grazie ad un maggior coordinamento delle iniziative. Si sottolinea come le azioni di miglioramento della qualità della prescrizione sono azioni complesse e di impatto variabili e richiedono sistemi di audit and feedback attivi per essere mantenute nel tempo. Si sottolinea la mancanza di un centro nazionale di riferimento sulla informazione indipendente che può rappresentare uno strumento nuovo e virtuoso (mai realizzato compiutamente in Italia) per allineare l’uso dei farmaci alle migliori evidenze disponibili e tale centro andrebbe disegnato e realizzato come uno strumento comune AIFA-SSN-Regioni.
- Appare evidente che sono molteplici le leve di intervento volte a garantire la sostenibilità della spesa già in essere o attuate da AIFA negli ultimi due anni. Ulteriori azioni potranno essere sviluppate di concerto tra AIFA e Regioni, e all’interno di un indirizzo politico e programmatico da parte dei ministeri vigilanti (MdS e MEF) preferibilmente nel triennio 2022-2024.
D’Amato (Lazio): “Piano attività manca di visione politica industriale”
Conferenza delle Regioni s Province autonome. Punto 7 all’odg del 28 settembre 2022: 7. Parere, ai sensi dell’articolo 48, comma 5, lettera h) del decreto legge 30 settembre 2003, n. 269, convertito, con modificazioni, dalla legge 24 novembre 2003, n. 326, sul programma di attività dell’Agenzia Italiana del Farmaco per l’anno 2022.
RINVIO





