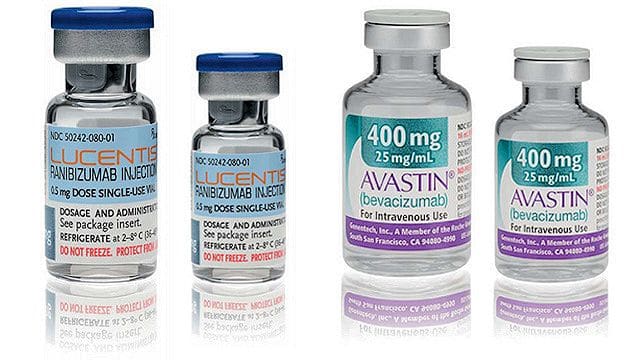
 L’Oms ha respinto la richiesta [di Novartis] e ha dato torto all’azienda con una motivazione che segue le ragioni della condanna dell’Antitrust: tra i farmaci utili per curare la maculopatia c’è già Avastin, “altrettanto efficace, sicuro ed economico”.
L’Oms ha respinto la richiesta [di Novartis] e ha dato torto all’azienda con una motivazione che segue le ragioni della condanna dell’Antitrust: tra i farmaci utili per curare la maculopatia c’è già Avastin, “altrettanto efficace, sicuro ed economico”.
Ma c’è qualcosa di più e di peggio in questa storia. Fatti che chiamano direttamente in causa l’Aifa, l’agenzia del farmaco, e lo stesso ministero della Salute. Perché nonostante la condanna dell’Antitrust, l’Aifa non solo non ha abbassato il prezzo del farmaco, ma non ha imposto alle strutture pubbliche di utilizzare il prodotto più economico. Permettendo così all’azienda di rientrare dei soldi – che non sappiamo se siano stati già pagati – della multa inflitta.
 si è dunque comportata in modo contraddittorio rispetto alla sentenza contro le multinazionali. Però è abbastanza ragionevole pensare che l’Agenzia abbia agito in accordo con il ministero della Salute.
si è dunque comportata in modo contraddittorio rispetto alla sentenza contro le multinazionali. Però è abbastanza ragionevole pensare che l’Agenzia abbia agito in accordo con il ministero della Salute.
Ma se fosse così saremmo alla schizofrenia, perché da una parte la ministra Lorenzin chiede alle aziende di pagare un danno subito dal suo ministero per 1,2 miliardi di euro, dall’altra favorisce la vendita del farmaco più costoso. Che assurdità è?
Non bastasse tutto questo, dal Corriere della Sera di oggi si scopre che Napoleone Ferrara, ricercatore di fama nominato dalla Lorenzin per il nuovo Consiglio superiore di Sanità, è lo scopritore dell’Avastin e del Lucentis.
(estratto da R.it Blog di Guglielmo Pepe)
Soi, senza paletti Aifa 300 mln l’anno per curare anche epatite C
 Piovella, con risparmi da maggiore uso Avastin si potrebbero pagare importanti terapie
Piovella, con risparmi da maggiore uso Avastin si potrebbero pagare importanti terapie
Se l’Aifa “intervenisse per risolvere la situazione ormai inspiegabile” legata all’uso dei farmaci Avastin e Lucentis contro le malattie degli occhi, “si potrebbero risparmiare circa 300 milioni di euro l’anno, da reinvestire in altri prodotti e interventi sanitari ‘salva-vista’, ad esempio per la cataratta, ma anche ‘salvavita’ come i nuovi medicinali contro l’epatite C”.
A tornare sul tema dei due trattamenti per la degenerazione maculare senile, uno molto meno caro dell’altro, oggetto di una maxi-multa alle due aziende produttrici Novartis e Roche accusate di aver fatto cartello a favore del secondo, è il presidente della Società oftalmologica italiana (Soi), Matteo Piovella. “La situazione sull’uso del farmaco meno caro in Italia, pur essendo iniziata ormai nel lontano 2007, quindi quasi 8 anni fa – evidenzia Piovella a Pharmakronos – è a tutt’oggi ancora molto complicata. Tutti hanno capito, in tutto il mondo, che non ci sono problemi di sicurezza legati all’uso di Avastin in oftalmologia”. Ultima, l’Organizzazione mondiale della sanità che non ha inserito il Lucentis nella lista dei farmaci innovativi. “Quei dubbi un po’ strumentali che si erano diffusi sono stati superati, anche se in tempi abbastanza lunghi”.
“ Lo stesso Napoleone Ferrara, inventore di tutti e due i medicinali – dice Piovella – tre settimane fa è stato invitato per un riconoscimento all’Università di Catania e durante la cerimonia ha ammesso che i due prodotti sono equivalenti e che uno deriva dall’altro. Una precisazione importante, dato che in passato le sue parole erano state invece usate a difesa del Lucentis. Tutto in teoria è semplice, le informazioni sono state comprese, ma muoiono nella burocrazia.
Lo stesso Napoleone Ferrara, inventore di tutti e due i medicinali – dice Piovella – tre settimane fa è stato invitato per un riconoscimento all’Università di Catania e durante la cerimonia ha ammesso che i due prodotti sono equivalenti e che uno deriva dall’altro. Una precisazione importante, dato che in passato le sue parole erano state invece usate a difesa del Lucentis. Tutto in teoria è semplice, le informazioni sono state comprese, ma muoiono nella burocrazia.
La normativa che ha messo in pista l’Aifa ha creato un imbuto molto ristretto, che ha fatto ridurre dell’80% l’uso di Avastin in Italia, mentre doveva dargli impulso. E’ una situazione kafkiana. Capisco che chi dà le regole voglia tutelare i farmaci approvati per un’indicazione precisa: l’uso off label sfugge dal controllo dell’ente regolatorio e questo ha creato confusione. Ma, senza motivazione, l’Aifa ha relegato l’uso di Avastin solo agli ospedali, mentre in tutto il mondo avviene in tutte le strutture. E gli oculisti negli ospedali italiani sono molto pochi: su 7.000, oggi sono in grado di prescrivere Avastin solo 100 specialisti. Poi, con un’altra normativa, sono state create delle difficoltà relative al frazionamento delle dosi, che avveniva a opera dei medici: è stata inserita l’obbligatorietà che a frazionare siano le farmacie ospedaliere, non tenendo conto che non sono attrezzate per farlo come vuole l’Aifa, e la maggioranza si rifiuta di farlo”.
Secondo Piovella, per risolvere la situazione “basterebbe tornare alla normativa in vigore prima del 2012, quando in seguito a rumors poi rivelatisi infondati l’Aifa è intervenuta con una serie di indicazioni e regole limitanti, che di fatto che hanno creato la situazione di oggi”. Problemi di sicurezza non ce ne sono, ribadisce la Soi: “Fin dal 2007 abbiamo emanato linee guida che obbligano a utilizzare queste terapie nelle sale operatorie. Chiediamo di essere messi in grado di usare il farmaco, abolendo le normative giustificate da un pericolo che si è rivelato inesistente”. In questi modo, calcola la Soi, si potrebbero generare ingenti risparmi, da reinvestire in cure delle malattie dell’occhio, ma anche per farmaci innovativi e molto costosi, come quelli per l’epatite C, che stanno creando problemi di sostenibilità al Ssn: “Una dose di Avastin costa circa 14 euro – spiega Piovella – una di Lucentis è arrivata da 2.500 a 600 euro.
E’ comunque di ben 40 volte più caro. I dati Ims dell’ultimo anno in Italia danno circa 170 milioni di euro di spesa per Lucentis più altri prodotti, per cui si arriva a 200 milioni. La spesa per Avastin è di soli 330.000 euro. E tenendo conto che oggi noi facciamo il 70% in meno di terapie rispetto ad altri Paesi europei, abbiamo calcolato che si potrebbero risparmiare 300 milioni di euro l’anno, che per un farmaco solo non sono pochi. Ma come mai, con un’attenzione così alta in questo periodo sulla spesa sanitaria e sul riassetto di tutto il sistema, non si affronta subito questa situazione? E’ inspiegabile”, conclude.