
L’UE si scontra con Big Pharma sul prezzo dei farmaci
Corriere PL –Di Diletta Fileni
Le riforme dell’Unione Europea mirano a far arrivare nuovi farmaci ai pazienti più velocemente e a un prezzo inferiore, ma questo è contro gli interessi di Big Pharma. Di conseguenza, le trattative sui prezzi dei medicinali stanno diventando ancora più complesse.
L’impennata delle spese mediche sta gravando sui bilanci globali con i leader di tutto il mondo che cercano di contenere l’inflazion, peraltro le pressioni sui prezzi stanno mettendo a dura prova la fornitura europea di medicinali più economici e senza brevetto. La questione è particolarmente delicata in Europa, poiché la domanda di assistenza sanitaria supera le aspettative e la guerra in Ucraina continua a far salire i prezzi di tutto, dall’energia ai beni di consumo.
L’UE si scontra con Big Pharma: perchè?
Il progetto di riforma prevede cambiamenti nella legislazione dell’industria farmaceutica dell’Unione europea (UE). Il piano è di abbreviare il periodo durante il quale le aziende farmaceutiche possono vendere i propri farmaci di marca senza concorrenza.
Al momento, le aziende che creano medicinali con una nuova formulazione possono commercializzarli per dieci anni senza timore che medicinali biosimilari entrino nel mercato.
N.d.R.: Il brevetto di un farmaco è il marchio di esclusiva dell’azienda farmaceutica produttrice. 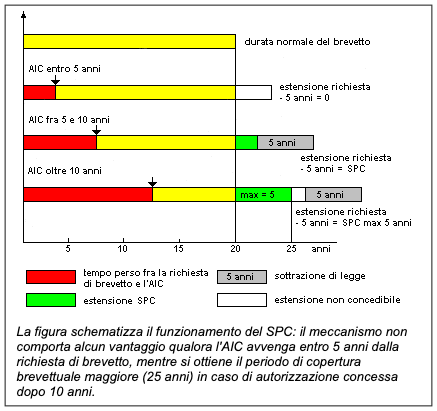 Il brevetto di un farmaco dura 20 anni (Legge Cee 1768 del 1992) e per tutto questo periodo, l’azienda farmaceutica che ha sviluppato il farmaco lo può commercializzare “in esclusiva”. Il brevetto non corrisponde necessariamente con l’immissione in commercio che può avvenire anche molti anni dopo. Nel caso dei farmaci infatti l’immissione in commercio è regolamentata da una procedura amministrativa che ha lo scopo di valutare la sicurezza e l’efficacia.Tenendo conto che occorrono almeno 10-12 anni perché un nuovo medicinale arrivi sul banco della Farmacia, questo significa che all’azienda rimangono solo 8 per ripagarne (complessivamente) 20. Per questa ragione, è stato istituito il “certificato di protezione supplementare” che è il titolo in forza del quale si prolunga la durata dell’esclusiva brevettuale per un periodo non superiore a 5 anni
Il brevetto di un farmaco dura 20 anni (Legge Cee 1768 del 1992) e per tutto questo periodo, l’azienda farmaceutica che ha sviluppato il farmaco lo può commercializzare “in esclusiva”. Il brevetto non corrisponde necessariamente con l’immissione in commercio che può avvenire anche molti anni dopo. Nel caso dei farmaci infatti l’immissione in commercio è regolamentata da una procedura amministrativa che ha lo scopo di valutare la sicurezza e l’efficacia.Tenendo conto che occorrono almeno 10-12 anni perché un nuovo medicinale arrivi sul banco della Farmacia, questo significa che all’azienda rimangono solo 8 per ripagarne (complessivamente) 20. Per questa ragione, è stato istituito il “certificato di protezione supplementare” che è il titolo in forza del quale si prolunga la durata dell’esclusiva brevettuale per un periodo non superiore a 5 anni
L’UE vuole accorciare questo periodo di due anni. Ciò significherebbe che i farmaci più economici saranno sul mercato prima e quindi accessibili a una popolazione più ampia.
Difatti una volta scaduto il brevetto di un farmaco, numerose aziende farmaceutiche offrono versioni generiche, che possono quindi ridurre il prezzo fino all’80-90%. Pertanto, la diminuzione della concorrenza spesso consente aumenti di prezzo, ma comporta anche un rischio più elevato di penuria di farmaci.
I cittadini europei hanno bisogno di accedere a prodotti e servizi sanitari innovativi e convenienti. Concorrenza effettiva significa che le aziende che producono prodotti farmaceutici, dispositivi sanitari o altri prodotti e servizi relativi alla salute competono tra loro sulla base della qualità e del prezzo dei loro prodotti e servizi. Di conseguenza, le aziende sono incentivate a investire nello sviluppo di nuovi trattamenti e ad applicare prezzi più competitivi.
Quando prevalgono tali circostanze, i cittadini vincono. D’altronde Big Pharma percepisce la notizia in  modo diverso. Dice che l’Europa è già in ritardo rispetto agli Stati Uniti e alla Cina nella ricerca e nello sviluppo di nuovi farmaci. Gli emendamenti previsti sono criticati anche da Nathalie Moll, direttore generale della Federazione europea delle industrie e delle associazioni farmaceutiche, che ha sottolineato che la riforma alla legislazione causerà enormi danni alla competitività dell’industria farmaceutica europea.
modo diverso. Dice che l’Europa è già in ritardo rispetto agli Stati Uniti e alla Cina nella ricerca e nello sviluppo di nuovi farmaci. Gli emendamenti previsti sono criticati anche da Nathalie Moll, direttore generale della Federazione europea delle industrie e delle associazioni farmaceutiche, che ha sottolineato che la riforma alla legislazione causerà enormi danni alla competitività dell’industria farmaceutica europea.
Mentre i dirigenti di Roche e Novartis hanno affermato questa settimana che vogliono che le autorità vedano la salute come un investimento invece che come un costo. Tuttavia, non è come se ogni speranza fosse persa per l’industria farmaceutica. Mancano ancora due mesi all’inoltro ufficiale delle modifiche legislative per l’approvazione, considerando che essa spende più di 40 milioni di euro ogni anno per influenzare le politiche dell’UE, impiegando circa 220 lobbisti.





