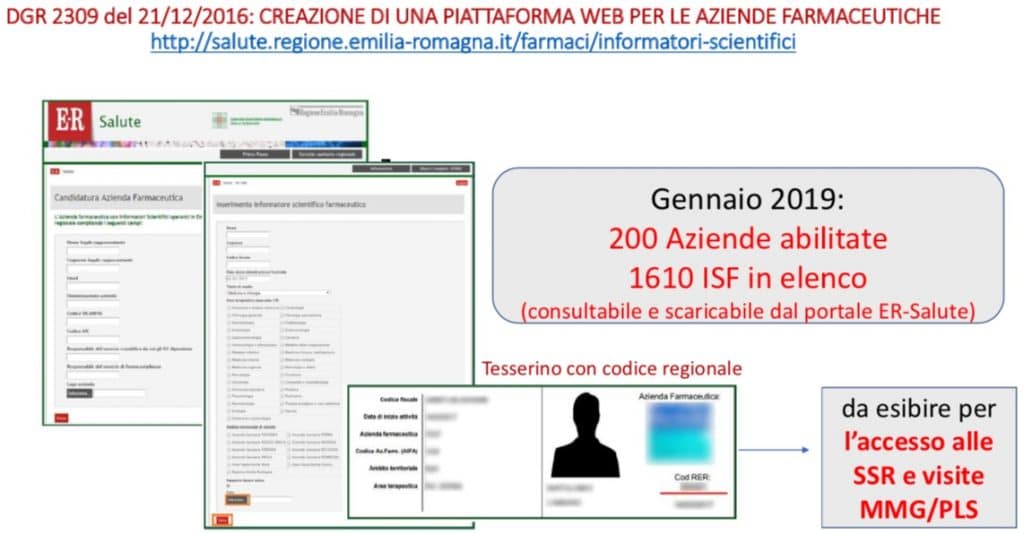
Il 21 ottobre scorso si è tenuto presso la sede della Regione Emilia Romagna l’incontro del Gruppo di lavoro sull’Informazione scientifica nell’ambito del SSR coordinato dalla Dr.ssa Valentina Solfrini, Dirigente di riferimento Area Farmaci e Dispositivi Medici della Direzione Generale Cura della Persona, Salute e Welfare dell’Assessorato Politiche della salute della Regione Emilia Romagna.
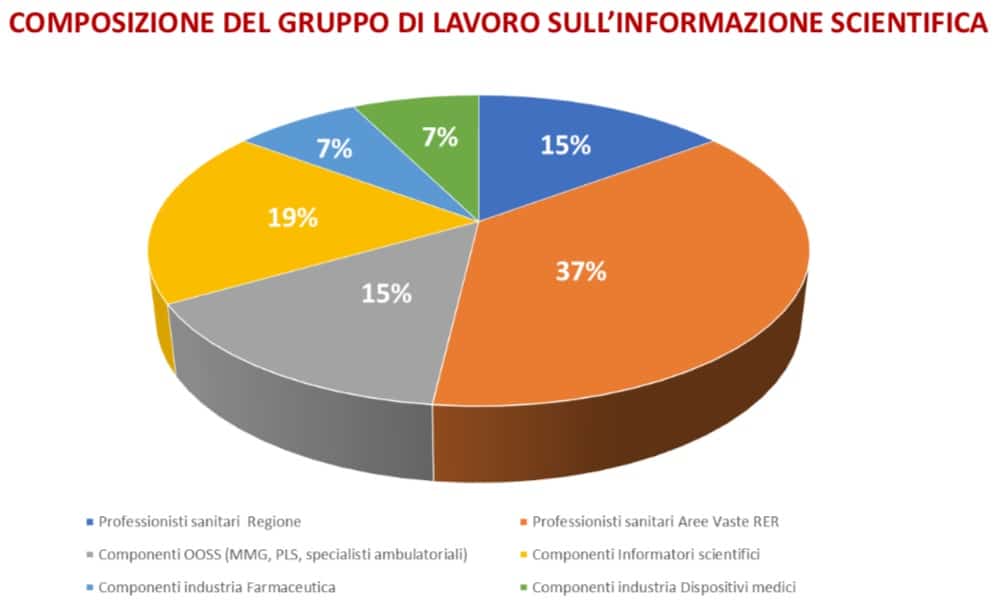 Occorre rimarcare il ruolo attivo di Fedaiisf la cui azione è stata fondamentale per evidenziare le criticità applicative del DGR 2309/2016 sulla regolamentazione dell’informazione scientifica, regolamento che sarebbe stato pericoloso per il futuro lavorativo di noi ISF
Occorre rimarcare il ruolo attivo di Fedaiisf la cui azione è stata fondamentale per evidenziare le criticità applicative del DGR 2309/2016 sulla regolamentazione dell’informazione scientifica, regolamento che sarebbe stato pericoloso per il futuro lavorativo di noi ISF
Grazie al contributo Fedaiisf il sistema sarà migliorato ed avvicinato a quella che è la realtà lavorativa.
Nel Gruppo di lavoro In rappresentanza degli Informatori Scientifici del Farmaco (ISF) era presente Fedaiisf il cui codice deontologico viene riconosciuto dalla Regione come valore. Anche per le rappresentanze sindacali erano presenti ISF.
Nell’incontro si è pensato ad un applicativo unico regionale che preveda l’inserimento dati personali, di argomento trattato, di professionista/i che si vuole/vogliono incontrare. E’ previsto anche l’avvenuto  incontro/i da parte dell’informatore, con possibilità e non l’obbligo da parte del medico di vedere in ogni momento chi lo vuole incontrare (e declinare nel caso) e chi dice di averlo incontrato (e negare nel caso). Il tutto non peserà né sulla operatività del medico, che se vuole può consultare il portale per visionare chi vuole vederlo e, eventualmente, riprogrammare l’incontro, né sull’operatività e autonomia gestionale dell’IS/ISF che deve, a posteriori, indicare quale medico ha visto, dove e quando.
incontro/i da parte dell’informatore, con possibilità e non l’obbligo da parte del medico di vedere in ogni momento chi lo vuole incontrare (e declinare nel caso) e chi dice di averlo incontrato (e negare nel caso). Il tutto non peserà né sulla operatività del medico, che se vuole può consultare il portale per visionare chi vuole vederlo e, eventualmente, riprogrammare l’incontro, né sull’operatività e autonomia gestionale dell’IS/ISF che deve, a posteriori, indicare quale medico ha visto, dove e quando.
E’ importante sottolineare il fatto che questo portale varrà per tutta la regione ed è previsto che entri in funzione nei primi mesi del 2020.
Riteniamo positivo l’esito dell’incontro e ci siamo lasciati con l’impegno che il Gruppo di Lavoro si incontri nuovamente entro metà novembre per valutare assieme ed eventualmente approvare un documento che affronti le Disposizioni tecniche e pratiche di applicazione del DGR 2309/2016 che meglio chiariscano gli aspetti di gestione degli incontri sia a livello territoriale (MMG, PLS, case della salute), sia a livello ospedaliero.
Riportiamo il resoconto dell’incontro:
Breve Resoconto incontro Gruppo di lavoro Informazione scientifica –
21 ottobre 2019
Il primo incontro del GdL coordinato dalla Dott.ssa Solfrini si apre con la presentazione dei componenti e dei loro ruoli.
 Vengono presentati anche gli obiettivi del GdL:
Vengono presentati anche gli obiettivi del GdL:
- individuare modalità operative omogenee di applicazione della DGR nelle singole aziende sanitarie con l’adozione di strumenti comuni possibilmente elettronici ma di semplice applicazione;
- valutare opportunità e strumenti per tracciare e valorizzare anche le attività di informazione sui dispositivi medici;
- condividere analisi e proposte relative alla promozione degli integratori nelle strutture sanitarie pubbliche.
con l’intenzione di svilupparli in un numero limitato di incontri.
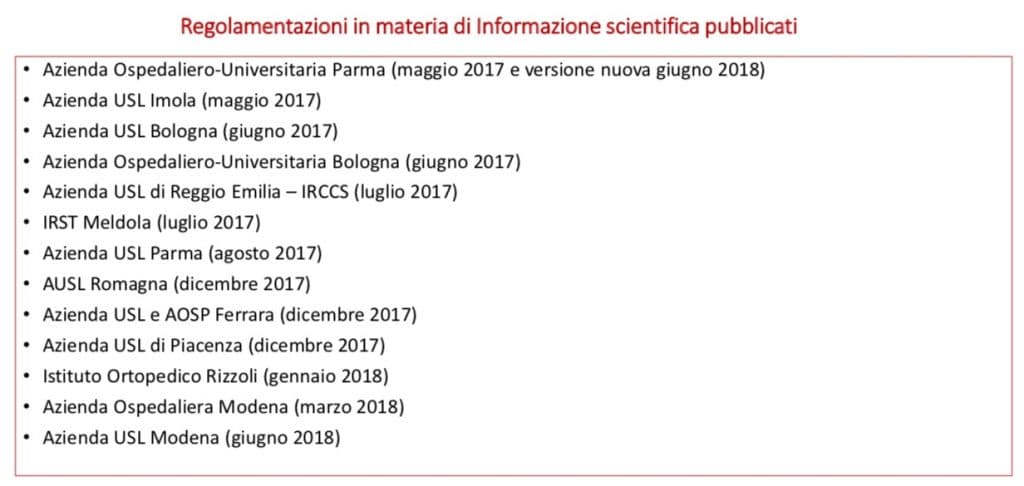 Si ripercorre il lavoro fatto in Regione Emilia Romagna negli anni recenti sul tema in oggetto, interrotto in previsione di una imminente uscita di nuove linee-guida di AIFA che non si è poi realizzata. Il lavoro di ricognizione e confronto già svolto negli anni sarà alla base delle proposte di modifica della DGR del 2016.
Si ripercorre il lavoro fatto in Regione Emilia Romagna negli anni recenti sul tema in oggetto, interrotto in previsione di una imminente uscita di nuove linee-guida di AIFA che non si è poi realizzata. Il lavoro di ricognizione e confronto già svolto negli anni sarà alla base delle proposte di modifica della DGR del 2016.
Viene ribadito che l’interesse della regione è quello di garantire trasparenza e tracciabilità a beneficio e valorizzazione dei rispettivi ruoli e dell’impegno dedicato a queste attività da parte di tutti i professionisti coinvolti, evitando che le procedure deliberate determinino un aggravio di compiti amministrativi o compilativi evitabili.
I componenti di parte regionale si impegnano a predisporre un applicativo elettronico di semplice compilazione che sarà reso disponibile in tutte le aziende entro i primi mesi del 2020, mantenendo la compilazione cartacea nel periodo di transizione.
Si ricorda che l’unica figura che ha specifiche regole di definizione del ruolo ed accesso è quella dell’informatore scientifico del farmaco (D.Lgs 219/2006), le altre figure non hanno una legislazione a supporto e potrebbero essere ricondotte ai portatori di interesse o ai promotori.
Sul tema Dispositivi medici si propone di distinguere il profilo di chi fa attività di addestramento da quella di informazione.
Notizie correlate: Emilia-Romagna.dgr-2309-2016
ANAC.Linee Guida Codice Comportamento SSN. per ISF pag. 10 (fondo pagina)