 Secondo l’OMS nel 2020 sono morti di cancro 10 milioni di persone. Per dare un’idea della dimensione di questa cifra si tenga presente che, sempre secondo l’OMS, i morti di Covid dall’inizio della pandemia a luglio 2023 sono stati 6.952.522. Secondo le stime dell’International Agency Research on Cancer (IARC), i casi di cancro nel mondo aumenteranno del 47 per cento nei prossimi 20 anni. Nel 2040 ci saranno 28,8 milioni di persone con una diagnosi di tumore, quasi il doppio di quelle attuali (19,3 milioni del 2020)
Secondo l’OMS nel 2020 sono morti di cancro 10 milioni di persone. Per dare un’idea della dimensione di questa cifra si tenga presente che, sempre secondo l’OMS, i morti di Covid dall’inizio della pandemia a luglio 2023 sono stati 6.952.522. Secondo le stime dell’International Agency Research on Cancer (IARC), i casi di cancro nel mondo aumenteranno del 47 per cento nei prossimi 20 anni. Nel 2040 ci saranno 28,8 milioni di persone con una diagnosi di tumore, quasi il doppio di quelle attuali (19,3 milioni del 2020)
La ricerca e gli studi clinici hanno consentito di compiere progressi importanti nello sviluppo di nuove terapie per la cura dei tumori. Nell’ultimo decennio la ricerca sul cancro ha fatto passi avanti da gigante. Terapie a bersaglio molecolare e l’immunoterapia hanno rivoluzionato il trattamento di molte neoplasie. Un traguardo possibile certamente grazie agli investimenti delle aziende farmaceutiche ma anche grazie al contributo della ricerca accademica non-profit.
Già avevamo segnalato l’innovativa terapia CAR-T (chimeric antigen receptor T cells) che, in estrema sintesi, si basa sul prelievo di linfociti T prelevati da un paziente affetto da tumore e modificate geneticamente in laboratorio in modo che reinfuse poi nello stesso paziente siano in grado di aggredire il tumore.
Ora ci sembra utile segnalare due promettenti ricerche. Una riguarda la tecnologia a mRNA e una riguarda la scoperta di una piccola molecola, AOH1996 (iniziali e anno di nascita di una bambina morta di tumore a 9 anni, Anna Olivia Healy, nel 2005, ndr) che uccide selettivamente le cellule tumorali.
 Ugur Sahin ed Ozlem Tureci (BioNTech), nel corso della cerimonia di chiusura dell’anno accademico 2022/2023, svoltasi a Roma, circa un mese fa, nella prestigiosa sede dell’Accademia dei Lincei , alla presenza del Presidente della Repubblica Sergio Mattarella, hanno illustrato la situazione attuale della ricerca scientifica BioNTech sui vaccini mRNA. Rispondendo alle domande dei giornalisti, al termine della cerimonia, il Prof. Ugur Sahin ha esposto i risultati di una ricerca, giunta alla fase della sperimentazione clinica, relativa all’attuazione di una terapia vaccinale personalizzata per alcune forme di tumore.
Ugur Sahin ed Ozlem Tureci (BioNTech), nel corso della cerimonia di chiusura dell’anno accademico 2022/2023, svoltasi a Roma, circa un mese fa, nella prestigiosa sede dell’Accademia dei Lincei , alla presenza del Presidente della Repubblica Sergio Mattarella, hanno illustrato la situazione attuale della ricerca scientifica BioNTech sui vaccini mRNA. Rispondendo alle domande dei giornalisti, al termine della cerimonia, il Prof. Ugur Sahin ha esposto i risultati di una ricerca, giunta alla fase della sperimentazione clinica, relativa all’attuazione di una terapia vaccinale personalizzata per alcune forme di tumore.
In pratica si procederebbe nel modo seguente. Dopo aver prelevato un campione cellulare dalla sede del tumore (o di una metastasi) si identificano le molecole maggiormente specifiche del tumore stesso, quindi si prepara il vaccino ad mRNA che stimola il sistema immunitario del malato per la produzione di linfociti killer ed anticorpi che aggrediscono e distruggono le cellule tumorali del malato.
L’immunoterapia è un tipo di trattamento del cancro che aumenta le difese naturali del corpo per combattere il cancro. Utilizza proteine prodotte dall’organismo o in laboratorio per addestrare il sistema immunitario del paziente a trovare e distruggere le cellule tumorali.
Tuttavia, ogni tipo di cancro è unico e crediamo, dice Ugur Sahin, che le immunoterapie dovrebbero essere in grado di affrontare ogni indicazione di cancro in modo diverso. Ecco perché abbiamo creato una gamma di piattaforme e strumenti tecnologici finalizzati allo sviluppo delle migliori opzioni terapeutiche per ogni indicazione tumorale.
Riteniamo che lo sfruttamento di modalità di azione complementari e potenzialmente sinergiche potrebbe aumentare la probabilità di successo terapeutico, ridurre il rischio di insorgenza di meccanismi di resistenza secondari e anche sbloccare una popolazione potenziale di pazienti più ampia.
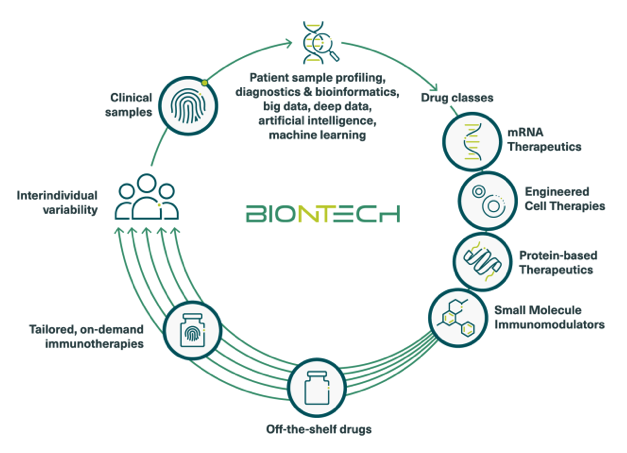 Stiamo sviluppando. conclude Sahim, attivatori immunitari basati su mRNA, cellule T mirate all’antigene, anticorpi e altre proteine terapeutiche come gli ADC [n.d.r.: coniugazione farmaco-anticorpo], nonché immunomodulatori definiti di varie risposte immunitarie. Questo portafoglio è progettato per rispecchiare gli effetti e l’evoluzione del sistema immunitario per fare affidamento su più percorsi complementari.
Stiamo sviluppando. conclude Sahim, attivatori immunitari basati su mRNA, cellule T mirate all’antigene, anticorpi e altre proteine terapeutiche come gli ADC [n.d.r.: coniugazione farmaco-anticorpo], nonché immunomodulatori definiti di varie risposte immunitarie. Questo portafoglio è progettato per rispecchiare gli effetti e l’evoluzione del sistema immunitario per fare affidamento su più percorsi complementari.
Nei nostri programmi terapeutici oncologici, entro la fine del 2022 abbiamo curato oltre 1.600 pazienti in più di 20 tipi di tumori solidi.
Cinque di questi programmi sono in fase di valutazione in studi randomizzati di Fase 2. Ricordiamo che gli studi clinici di fase 2 sono progettati per studiare la sicurezza e la tollerabilità del farmaco candidato in un gruppo più ampio di individui, rispetto alla fase 1 (di solito fino a 100 per trattamento), e per valutare l’efficacia precoce del prodotto candidato nella popolazione target.
BNT211 comprende due prodotti farmaceutici, una terapia cellulare CAR-T autologa mirata all’antigene oncofetale Claudin-6 (CLDN6) e un vaccino a RNA CAR-T codificante CLDN6 (CARVac) basato sulla tecnologia proprietaria di BioNTech mRNA-lipoplex per migliorare la persistenza e funzionalità delle cellule CAR-T. La terapia mira a indurre una potente risposta immunitaria contro vari tumori solidi CLDN6+, come il cancro ovarico, il sarcoma, il cancro ai testicoli, il cancro dell’endometrio e il cancro gastrico. È un potenziale approccio terapeutico di prim’ordine e il prodotto candidato CAR-T più avanzato nello sviluppo clinico di BioNTech. BNT211 è attualmente in fase di studio da solo o in combinazione con CARVac in uno studio di fase 1/2 in pazienti con tumori solidi avanzati recidivanti o refrattari al CLDN6+. I primi risultati preliminari hanno dimostrato un profilo di sicurezza incoraggiante e primi segni di efficacia antitumorale ai primi livelli di dose valutati di BNT211.
La seconda scoperta, dopo 20 anni di ricerca e sviluppo condotti dal City of Hope Hospital di Los Angeles, che, se conferma l’efficacia sull’uomo, è destinata a rivoluzionare l’approccio terapeutico al cancro è  AOH1996 (nome in codice).
AOH1996 (nome in codice).
Per comprendere il meccanismo d’azione di AOH1996 occorre conoscere PCNA. PCNA è una proteina omotrimerica nucleare che circonda il DNA con attributi classici di un fattore di processività nella replicazione del DNA.
L’antigene nucleare cellulare proliferante (PCNA, Proliferating cell nuclear antigen) è un fattore centrale nei percorsi di replicazione e riparazione del DNA che svolge un ruolo essenziale nella stabilità del genoma. I ruoli funzionali del PCNA sono mediati da un ampio elenco di interazioni proteina-proteina, ognuna delle quali trasmette informazioni specifiche negli assemblaggi proteici. La flessibilità delle interfacce di interazione PCNA-proteina offre opportunità per la scoperta di inibitori funzionalmente selettivi delle vie di riparazione del DNA.
Attualmente si propone che più di 200 proteine interagiscano con il PCNA con un importante sottoinsieme coinvolto nella riparazione del danno del DNA. Molte proteine chiave condividono un “motivo” di legame per il PCNA chiamate “motivo simile a una proteina che interagisce con il PCNA (PIPM).
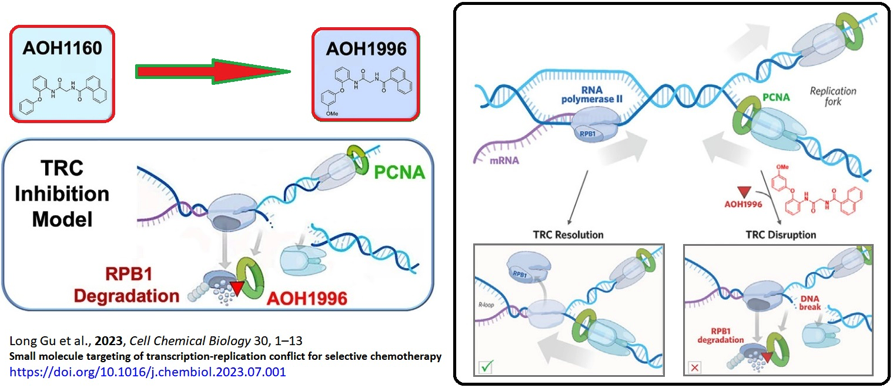
 La chimica farmaceutica diretta dalla cristallografia identifica un ligando PCNA che stabilizza l’interazione tra il PCNA legato alla cromatina e la subunità più grande RBP1 (La subunità RPB1 dell’RNA polimerasi II diretta dal DNA dell’RNA polimerasi II), portando alla degradazione dell’RPB1 intracellulare. e interferisce con la risoluzione TRC (Transcription-replication conflicts).
La chimica farmaceutica diretta dalla cristallografia identifica un ligando PCNA che stabilizza l’interazione tra il PCNA legato alla cromatina e la subunità più grande RBP1 (La subunità RPB1 dell’RNA polimerasi II diretta dal DNA dell’RNA polimerasi II), portando alla degradazione dell’RPB1 intracellulare. e interferisce con la risoluzione TRC (Transcription-replication conflicts).L’interazione PCNA e RBP1 crea una vulnerabilità selettiva per il cancro. I risultati suggeriscono la potenziale utilità di AOH1996 anche come strumento chimico per definire ulteriormente i TRC nelle cellule e dimostrano chiaramente il potenziale terapeutico di AOH1996 quando viene utilizzato come monoterapia, nonché quando viene utilizzato in combinazione con chemioterapie esistenti.
AOH1996 induce pertanto rotture a doppio filamento del DNA in modo dipendente dalla trascrizione.
Somministrato per via orale, l’AOH1996 sopprime la crescita tumorale ma non provoca effetti collaterali distinguibili. In sostanza impedisce alle cellule con DNA danneggiato di dividersi e blocca la replicazione del DNA difettoso. Questa combinazione di fattori porta alla morte delle cellule tumorali, senza danneggiare le cellule sane durante il processo.
AOH1160 (uno degli analoghi a AOH1996) presenta notevoli proprietà terapeutiche: è somministrabile per via orale in una formulazione compatibile con il suo uso clinico, e negli studi sugli animali inibisce quasi completamente la crescita dei tumori xenotrapiantati e li sensibilizza all’inibizione della topoisomerasi (ndr: enzimi che riuniscono le estremità interrotte di DNA). Negli studi che seguono le linee guida di buona pratica di laboratorio (BPL) della Food and Drug Administration (FDA) statunitense, l’AOH1996 non provoca alcuna tossicità percepibile a 6 o più volte la dose efficace nei topi e nei cani.
 Semplificando AOH1996 colpisce una variante specifica di PCNA che si trova esclusivamente nelle cellule tumorali, interrompendo il loro normale ciclo riproduttivo. Seguendo solo tale variante, può essere possibile colpire selettivamente solo le cellule tumorali.
Semplificando AOH1996 colpisce una variante specifica di PCNA che si trova esclusivamente nelle cellule tumorali, interrompendo il loro normale ciclo riproduttivo. Seguendo solo tale variante, può essere possibile colpire selettivamente solo le cellule tumorali.
Da agosto 2023 è in studio clinico di fase 1 (che fornisce elementi preliminari per una valutazione della sicurezza del principio attivo e per accertarne la tolleranza dell’organismo in un numero limitato di persone) per il trattamento dei tumori solidi.
In particolare, il farmaco è stato testato su oltre 70 linee di cellule tumorali, tra cui quelle derivanti da cancro al seno, alla prostata, al cervello, alle ovaie, al collo dell’utero, alla pelle e ai polmoni. E il risultato è stato stupefacente: la pillola si è dimostrata efficace contro tutte le tipologie di tumori prese in esame.
È ancora troppo presto per dire che avremo a breve una terapia universale contro il cancro. Non è scontato infatti che il farmaco non possa arrestarsi prima in una delle 3 fasi delle sperimentazioni cliniche, perché non soddisfa gli obiettivi richiesti.
Ovviamente occorre che un’azienda farmaceutica finanzi le sperimentazioni cliniche, e che ne finanzi la produzione, se superate le 3 fasi, previa autorizzazione delle Agenzie governative competenti in ciascun Paese interessato: siano la FDA, l’EMA, l’Aifa, o altro ente regolatorio. Un percorso irto di ostacoli, che richiederà ancora parecchi anni.
Le notizie di queste scoperte sono arrivate alla “stampa laica” con conseguente sensazionalismo e clamore.
La comunicazione di questi messaggi così delicati quando sono rivolti ad un pubblico culturalmente non attrezzato ha bisogno di maggiore prudenza, sensibilità, conoscenza, chiarezza. Bisogna spiegare bene che le scoperte di cui si parla appartengono al futuro e al probabile. Sono precisazioni che chi informa deve fare per rispetto dei malati, dei loro cari, dei loro oncologi curanti, delle verità che i ricercatori meritano perché non si equivochi su di loro.
Se AOH1996 si dimostrerà efficace e sicura negli esseri umani anche nelle successive fasi, come lo è stata nei test di laboratorio, potrebbe rappresentare una sensazionale svolta nella terapia del cancro. La prudenza però nel creare speranze e aspettative eccessive è fondamentale.
Notizie correlate:
Cell – Gu et al., 2023, Cell Chemical Biology 30, 1–13
Pillola contro Tutti i Tumori: Una svolta rivoluzionaria nell’Oncologia
New PCNA inhibitor AOH1996 shows selective cancer cell killings and tumor suppression potential
«Così combattiamo i tumori», viaggio nei laboratori dell’Istituto oncologico veneto





