Come si trasmette la malaria
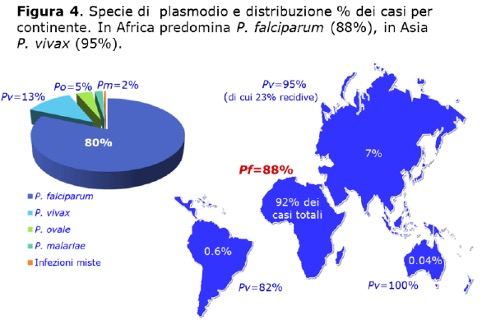
 È la zanzara anofele a trasmettere la malaria ma non è l’insetto stesso a causare la malattia. La malaria è causata da differenti tipologie di plasmodio (6 tipi: falciparum, vivax, ovale curtisi, ovale wallikeri, malariae, knowlesi), organismi unicellulari appartenenti al regno dei protozoi. Per compiere il loro ciclo vitale devono necessariamente replicarsi all’interno dei globuli rossi dell’uomo. Ciò avviene quando la zanzara anofele, tramite una puntura, rilascia dalle sue ghiandole salivari il plasmodio che è così libero di entrare nel circolo sanguigno della persona punta dall’insetto. Allo stesso modo, sempre mediante puntura, il plasmodio può tornare nuovamente nella zanzara e andare ad infettare un’altra persona punta successivamente.
È la zanzara anofele a trasmettere la malaria ma non è l’insetto stesso a causare la malattia. La malaria è causata da differenti tipologie di plasmodio (6 tipi: falciparum, vivax, ovale curtisi, ovale wallikeri, malariae, knowlesi), organismi unicellulari appartenenti al regno dei protozoi. Per compiere il loro ciclo vitale devono necessariamente replicarsi all’interno dei globuli rossi dell’uomo. Ciò avviene quando la zanzara anofele, tramite una puntura, rilascia dalle sue ghiandole salivari il plasmodio che è così libero di entrare nel circolo sanguigno della persona punta dall’insetto. Allo stesso modo, sempre mediante puntura, il plasmodio può tornare nuovamente nella zanzara e andare ad infettare un’altra persona punta successivamente.
La cura della malattia
L’intervento precoce è la miglior arma per combattere la malaria. In precedenza non esisteva un vaccino e la strategia più utilizzata era la profilassi farmacologica, un trattamento che è possibile svolgere sia in chiave 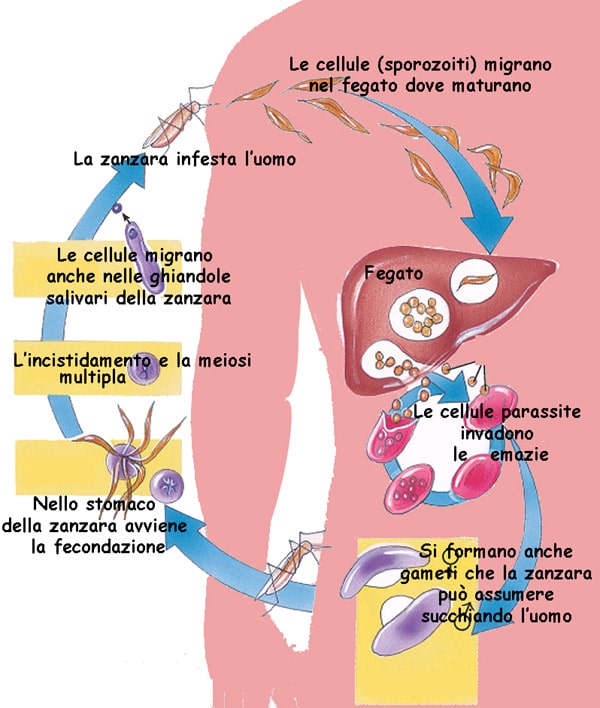 preventiva sia come terapia vera e propria. Uno dei primi farmaci in commercio è stato l’artemisina -molecola attiva contro il plasmodio. Il farmaco viene utilizzato in casi estremamente gravi di malaria e viene somministrato per via endovenosa o intramuscolare. Normalmente si può usare Chinina in associazione con doxiciclina, clorochina, idrossiclorochina (Plaquenil), meflochina, ecc..
preventiva sia come terapia vera e propria. Uno dei primi farmaci in commercio è stato l’artemisina -molecola attiva contro il plasmodio. Il farmaco viene utilizzato in casi estremamente gravi di malaria e viene somministrato per via endovenosa o intramuscolare. Normalmente si può usare Chinina in associazione con doxiciclina, clorochina, idrossiclorochina (Plaquenil), meflochina, ecc..
Il vaccino
Il Comitato dell’Agenzia europea per i medicinali per uso umano (CHMP) ha rilasciato un parere scientifico positivo per Mosquirix di GSK, il primo vaccino umano contro la malaria noto anche come RTS, S / AS01. Il medicinale, è il risultato di 30 anni di ricerca ed il suo meccanismo d’azione innesca una risposta immunitaria durante le prime fasi dell’infezione da parte del parassita plasmodium falciparum. Entra in azione subito dopo la puntura della zanzara anofele, quando il microrganismo entra nel flusso sanguigno. L’obiettivo è quello di difendere l’organismo e impedire il radicamento della malattia.
L’Organizzazione mondiale della sanità (Oms) ha approvato Mosquirix il 6 ottobre come primo vaccino contro la malaria per un uso diffuso, mossa che gli esperti sperano possa salvare decine di migliaia di vite di bambini in tutta l’Africa. ll vaccino è stato sottoposto a lunghi studi clinici. È stato sperimentato in 7 paese africani ma i risultati ottenuti non sono stati quelli sperati: infatti si è visto che è stato possibile prevenire la malaria nel 56% dei bambini tra 7 e i 17 mesi e solo nel 31% dei bimbi tra le 6 e le 12 settimane. La combinazione della chemioprevenzione stagionale con la vaccinazione stagionale con RTS,S/AS01 fornisce un approccio promettente alla prevenzione della malaria nelle vaste aree dell’Africa con malaria stagionale e dove la malaria è attualmente scarsamente controllata. L’efficacia del vaccino è diminuita dopo un anno. Sulla base dei risultati della sperimentazione il CHMP ha concluso che, nonostante la sua limitata efficacia, i benefici di Mosquirix superano i rischi. Fino ad oggi sono state somministrate più di 2,3 milioni di dosi del vaccino in paesi africani ed ha dimostrato un profilo di sicurezza favorevole. Va somministrato in quattro dosi a partire dai cinque mesi di età. La seconda e la terza a distanza di un mese ciascuna e l’ultima a 18 mesi.
Il vaccino contro la malaria è una proteina ricombinante, che è la proteina superficiale del circumsporozoite, il protozoo che viene inoculato dalla puntura dell’insetto. Il plasmodio migra poi al fegato, e nel fegato si moltiplica, infetta i globuli rossi e provoca gli effetti della malattia. Il vaccino è un antigene coniugato con l’antigene di superficie del virus dell’epatite B (per renderlo ancora più forte) e ha un adiuvante molto potente che sono dei liposomi, cioè delle particelle di lipidi che contengono al loro interno un agonista del Toll-like receptor 4, un recettore che attiva la risposta immuno-infiammatoria.
 Il “Gene Drive”, prospettive future
Il “Gene Drive”, prospettive future
E in futuro un ulteriore strumento nella lotta contro la malaria, potrebbero essere le tecniche di gene drive attraverso le quali si cercherà di controllare le popolazioni di insetti vettori attraverso la modificazione del loro genoma. È una biotecnologia che sta venendo messa a punto, tra gli altri laboratori, da Andrea Crisanti. L’idea nasce nel 2000 quando per la prima volta Flaminia Catteruccia, ricercatrice italiana dell’Imperial College (oggi trasferitasi a Harvard), riesce a modificare stabilmente il genoma di una zanzara (Anopheles stephensi). Due anni più tardi si ottiene il genoma completo dell’insetto e nel 2003 gli studi di un professore canadese dell’Imperial College, Austin Burt, spalancano le porte alla realizzazione di idee che per 40 anni erano state solo fantascienza: controllare le popolazioni di insetti vettori attraverso la modificazione del loro genoma.
Notizie correlate: Seasonal Malaria Vaccination with or without Seasonal Malaria Chemoprevention
WHO recommends groundbreaking malaria vaccine for children at risk
Malaria, cosa significa avere finalmente un vaccino





